EP1694829B1.pdf
Aperçu texte
EP 1 694 829 B1
5
10
15
20
Phase solide (Acm 166 + 87 région centrale) : conjugué anticorps 28 (C-ter)
2. Combinaison G/28
Phase solide (Acm 86 - épitope conformationel) : conjugué anticorps 28 (C-ter)
3. Combinaison H/28
Phase solide (Acms 86, 166 et 87 région centrale et épitope conformationel) : conjugué anticorps 28 (C-ter)
4. Combinaison H/28 + 87
Phase solide (Acms 86, 166 et 87 région centrale et épitope conformationel) : conjugué mixte anticorps 28 (C-ter)
et 87 (central)
5. Combinaison G/87
Phase solide (Acm 86 - épitope conformationel) : conjugué anticorps 87 (région centrale)
Les 4 premières combinaisons présentent des performances équivalentes et reproduites, supérieures aux autres
combinaisons mises en oeuvre (comme par exemple la combinaison G/87). Bien entendu, dans ces combinaisons,
un anticorps monoclonal peut être remplacé par un autre anticorps reconnaissant le même épitope. Ainsi, on peut
citer les variantes suivantes :
6. Variante de la combinaison F/28
Phase solide (Acm 87 uniquement) : conjugué anticorps 57 (C-ter)
7. Variante de la combinaison G/28
Phase solide (Acm 86 - épitope conformationel) : conjugué anticorps 57 (C-ter)
8. Variante de la combinaison H/28
Phase solide (Acms 86 et 87 région centrale et épitope conformationel) : conjugué anticorps 57 (C-ter)
9. Variante de la combinaison H/28 + 87
Phase solide (Acms 86 et 87 région centrale et épitope conformationel) : conjugué mixte anticorps 57 (C-ter) et 87
(central)
25
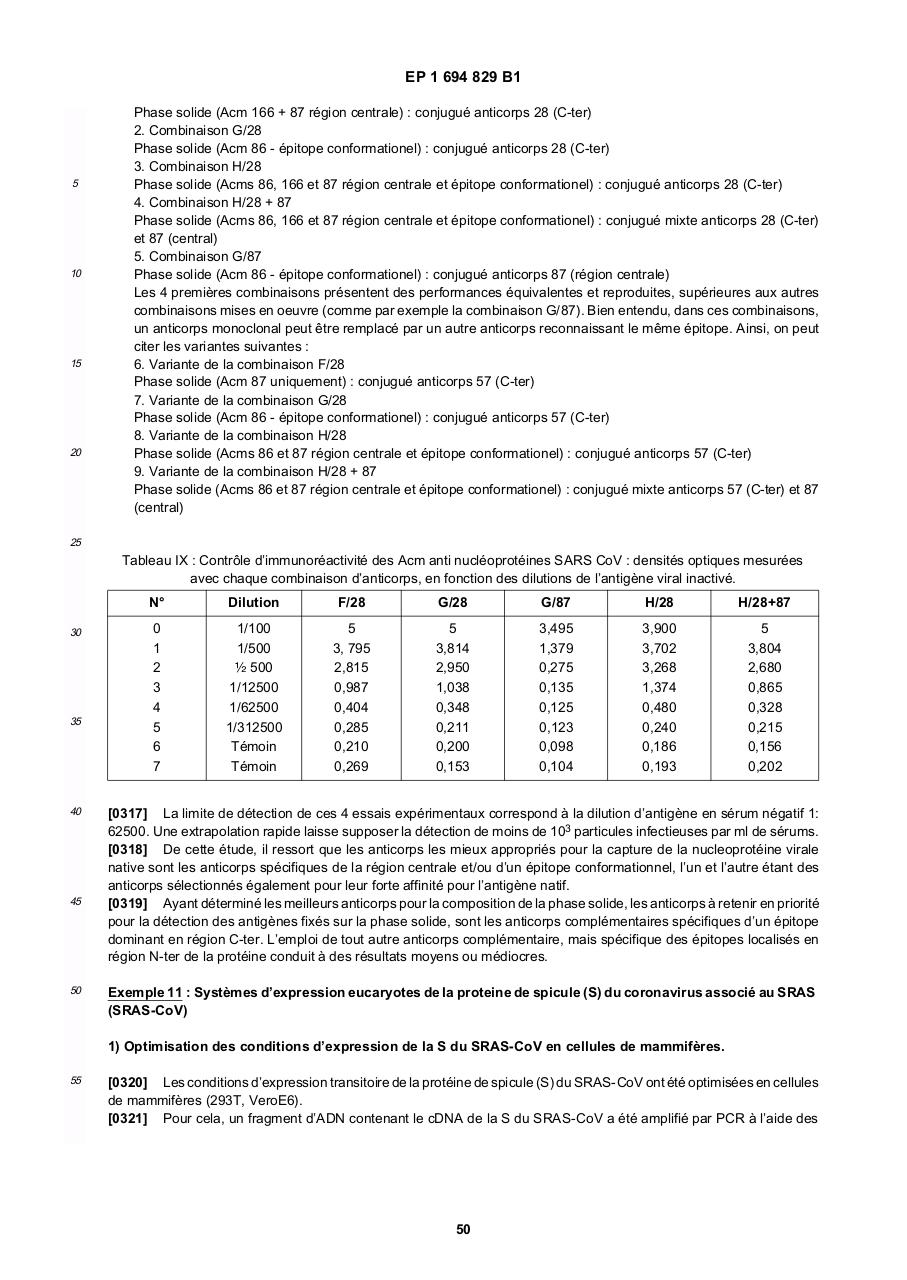
Tableau IX : Contrôle d’immunoréactivité des Acm anti nucléoprotéines SARS CoV : densités optiques mesurées
avec chaque combinaison d’anticorps, en fonction des dilutions de l’antigène viral inactivé.
30
35
40
45
50
N°
Dilution
F/28
G/28
G/87
H/28
H/28+87
0
1
2
3
4
5
6
7
1/100
1/500
500
1/12500
1/62500
1/312500
Témoin
Témoin
5
3, 795
2,815
0,987
0,404
0,285
0,210
0,269
5
3,814
2,950
1,038
0,348
0,211
0,200
0,153
3,495
1,379
0,275
0,135
0,125
0,123
0,098
0,104
3,900
3,702
3,268
1,374
0,480
0,240
0,186
0,193
5
3,804
2,680
0,865
0,328
0,215
0,156
0,202
[0317] La limite de détection de ces 4 essais expérimentaux correspond à la dilution d’antigène en sérum négatif 1:
62500. Une extrapolation rapide laisse supposer la détection de moins de 103 particules infectieuses par ml de sérums.
[0318] De cette étude, il ressort que les anticorps les mieux appropriés pour la capture de la nucleoprotéine virale
native sont les anticorps spécifiques de la région centrale et/ou d’un épitope conformationnel, l’un et l’autre étant des
anticorps sélectionnés également pour leur forte affinité pour l’antigène natif.
[0319] Ayant déterminé les meilleurs anticorps pour la composition de la phase solide, les anticorps à retenir en priorité
pour la détection des antigènes fixés sur la phase solide, sont les anticorps complémentaires spécifiques d’un épitope
dominant en région C-ter. L’emploi de tout autre anticorps complémentaire, mais spécifique des épitopes localisés en
région N-ter de la protéine conduit à des résultats moyens ou médiocres.
Exemple 11 : Systèmes d’expression eucaryotes de la proteine de spicule (S) du coronavirus associé au SRAS
(SRAS-CoV)
1) Optimisation des conditions d’expression de la S du SRAS-CoV en cellules de mammifères.
55
[0320] Les conditions d’expression transitoire de la protéine de spicule (S) du SRAS-CoV ont été optimisées en cellules
de mammifères (293T, VeroE6).
[0321] Pour cela, un fragment d’ADN contenant le cDNA de la S du SRAS-CoV a été amplifié par PCR à l’aide des
50